2021年10月8日,西湖大学徐和平及何丹阳共同通讯在Immunity 在线发表题为“Early developing B cells undergo negative selection by central nervous system-specific antigens in the meninges”的研究论文,该研究确定了小鼠和非人类灵长类动物脑膜中 B 细胞发育的连续轨迹。
脑膜 B 细胞主要位于硬脑膜窦,在那里内皮细胞表达支持 B 细胞发育的必要生态位因子。
联体共生实验和谱系追踪表明,脑膜发育中的 B 细胞通过不依赖循环的途径从造血干细胞 (HSC) 衍生的祖细胞中不断补充。
识别髓鞘少突胶质细胞糖蛋白 (MOG)(一种中枢神经系统特异性抗原)的自身反应性未成熟 B 细胞被专门从脑膜中清除。
此外,Mog 基因的遗传缺失恢复了脑膜中的自我反应性 B 细胞群。
这些发现将脑膜确定为 B 细胞发育的独特储存库,允许原位负选择以确保局部非自身反应性免疫组库。
免疫球蛋白 (Ig) 基因座的随机 V(D)J 重组通常会产生表达自我识别 B 细胞受体 (BCR) 的自身反应性 B 细胞,这些受体通过自身抗原依赖性中枢和外周耐受性被消除或灭活检查点以防止自身免疫反应。
然而,当高度组织特异性的自身抗原——例如髓鞘少突胶质细胞糖蛋白 (MOG)——一种仅在中枢神经系统 (CNS) 中表达的糖蛋白的局部浓度不足时,为了在骨髓 (BM) 和脾脏中启动负选择,自身反应性 B 细胞可以逃避这些耐受检查点并持续存在于成熟的 B 细胞库中。
长期以来,大脑一直被认为是具有免疫豁免的器官,由于缺乏淋巴引流和免疫细胞无法到达,因此无法发起有效的免疫反应。
然而,由于在稳态条件下(重新)发现脑膜淋巴管,这一传统概念已被修改。
脑膜已成为活跃的神经免疫界面,其中包含大量免疫细胞,这些细胞介导脑膜免疫并参与不同的神经炎症状况,包括嗜神经性感染和多发性硬化症。
单细胞分析研究表明,B 细胞存在于小鼠的脑膜中。
最近的工作还表明,脑膜含有未成熟和成熟的 B 细胞。
尽管取得了这些进展,但这些 B 细胞对中枢神经系统的脑膜免疫和免疫稳态的贡献在很大程度上是未知的。
特别是,自身反应性未成熟和成熟 B 细胞识别中枢神经系统特异性抗原,这些抗原逃脱了 BM 和脾脏中的耐受检查点,也可能存在于脑膜中。
因此,自身反应性 B 细胞是否以及如何对脑膜中的 CNS 特异性抗原作出反应仍有待阐明。
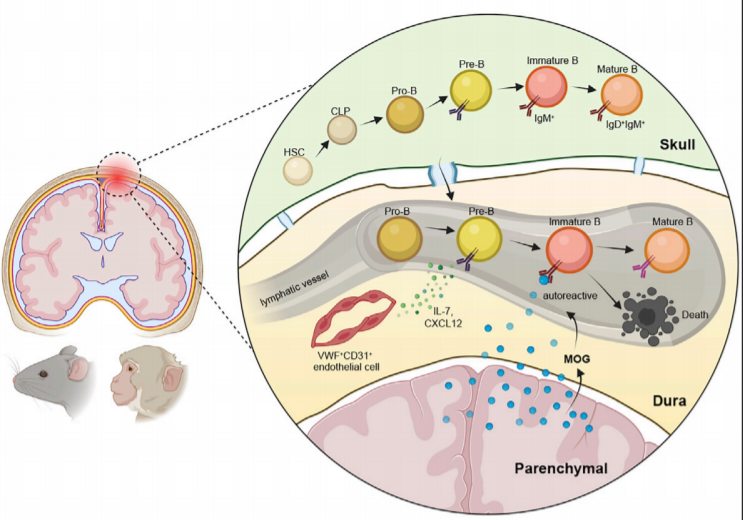
脑膜B淋巴细胞发育与阴性筛选研究总结示意图(图源自Immunity )该研究使用大规模平行单细胞 RNA 测序 (scRNA-seq) 分析来揭示小鼠脑膜发育 B 细胞的连续轨迹(跨越原始到未成熟的 B 细胞),这证实了最近的两项研究。
在非人类灵长类动物 (NHP) 的脑膜中也发现了相同的 B 细胞发育轨迹。
造血干细胞 (HSC) 的谱系追踪表明,脑膜发育中的 B 细胞不断从 HSC 衍生的祖细胞中得到补充。
Parabiotic 小鼠模型进一步证明,脑膜发育中 B 细胞的补充途径与循环无关。
MOG 蛋白存在于脑膜中,但不存在于颅骨、胫骨、股骨或脾脏中。
重要的是,识别 MOG 的未成熟 B 细胞在 IgHMOG 敲入小鼠(也称为 Th 小鼠)的脑膜中被特异性清除。
与这些结果一致,Mog 基因的缺失恢复了脑膜中的自我反应性 B 细胞群。
总的来说,该研究数据表明,脑膜作为 B 细胞发育的独特储存库,允许对 CNS 抗原自身反应性 B 细胞进行原位阴性选择,作为额外的检查点层,以严格维持局部非自身反应性免疫微环境。
西湖大学徐和平和何丹阳研究员为论文共同通讯作者,西湖大学博士研究生王琰、陈钿雨和科研助理徐的为本文共同第一作者。
本项目受到科技部重点研发计划、国家自然基金委、西湖实验室以及西湖教育基金会的资助;项目实施过程中得到了西湖大学实验动物中心、流式平台、基因组学平台以及超算平台的大力支持。
原文链接:https://www.cell.com/immunity/fulltext/S1074-7613(21)00401-5 来源:iNature网站:www.cscb.org.cn微信:CSCB-WeChat扫码关注我们





 微信公众号
微信公众号
 下载app
下载app
 京公网安备 11010202008974号
京公网安备 11010202008974号