来源:高分子科学前沿
人体内特殊部位的压力,是监测人体各种严重甚至致命的医学状态的关键诊断参数,包括颅内、腹腔内和肺动脉高压等。商用的植入式传感器在测量压力方面提供了较好的准确性和稳定性,但在患者康复后需要手术切除,以避免感染和其他的风险。可溶解在生物体液环境中的传感器(或生物可吸收的传感器)可避免此类手术的需要,但目前的设计大多涉及硬接线连接,无法在临床寿命内提供定量测量。日前,美国西北大学Rogers教授带领的团队研制了一种基于无源电感电容谐振电路的生物可吸收无线压力传感器,其结构布局和材料组合克服了这些缺点。该传感器经过优化设计,灵敏度最高可达到200 kHz mmHg−1,分辨率可达到1mmHg。使用Si3N4膜和天然蜡封边的包封方法,可实现在体内长达4天的稳定工作。相关工作以“Bioresorbable Wireless Sensors as Temporary Implants for In Vivo Measurements of Pressure”发表在《Advanced Functional Meterials》。 图1:用于体内压力测量的临时植入式生物可吸收无线传感器工作机理:
图1:用于体内压力测量的临时植入式生物可吸收无线传感器工作机理: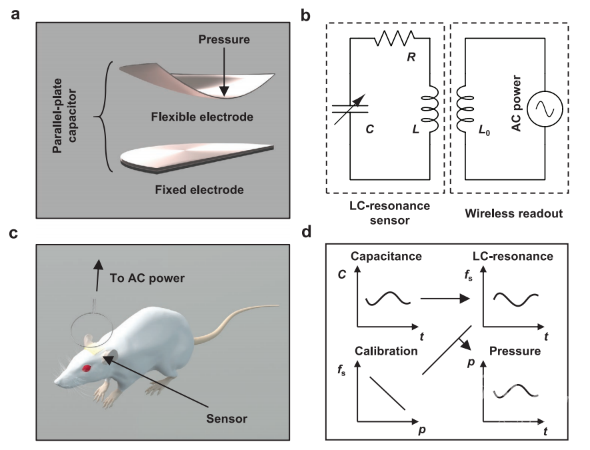 图2:可吸收、被动、无线压力传感器的原理图、电路图、工作原理和动物模型应用。a)具有柔性和固定电极的平行板电容器的结构示意图,以产生与压力相关的电容C。b) LC谐振传感器与无线读出系统的等效电路。c) 颅内压无线传感示意图基于与外部读出线圈耦合的植入LC谐振传感器。d) 信号转换过程的流程图。其工作原理基于谐振电路(LC电路)的无线压力传感器。可变形的导电膜将周围流体的压力转化为机械响应。将这种薄膜与固定电极配对形成平行板电容器,进而将这种弯曲变形转化为电容的变化(如图2所示)。而电容的变化还会导致电路的谐振频率发生变化,这可以通过与外部天线的无线耦合来检测。工艺过程:
图2:可吸收、被动、无线压力传感器的原理图、电路图、工作原理和动物模型应用。a)具有柔性和固定电极的平行板电容器的结构示意图,以产生与压力相关的电容C。b) LC谐振传感器与无线读出系统的等效电路。c) 颅内压无线传感示意图基于与外部读出线圈耦合的植入LC谐振传感器。d) 信号转换过程的流程图。其工作原理基于谐振电路(LC电路)的无线压力传感器。可变形的导电膜将周围流体的压力转化为机械响应。将这种薄膜与固定电极配对形成平行板电容器,进而将这种弯曲变形转化为电容的变化(如图2所示)。而电容的变化还会导致电路的谐振频率发生变化,这可以通过与外部天线的无线耦合来检测。工艺过程: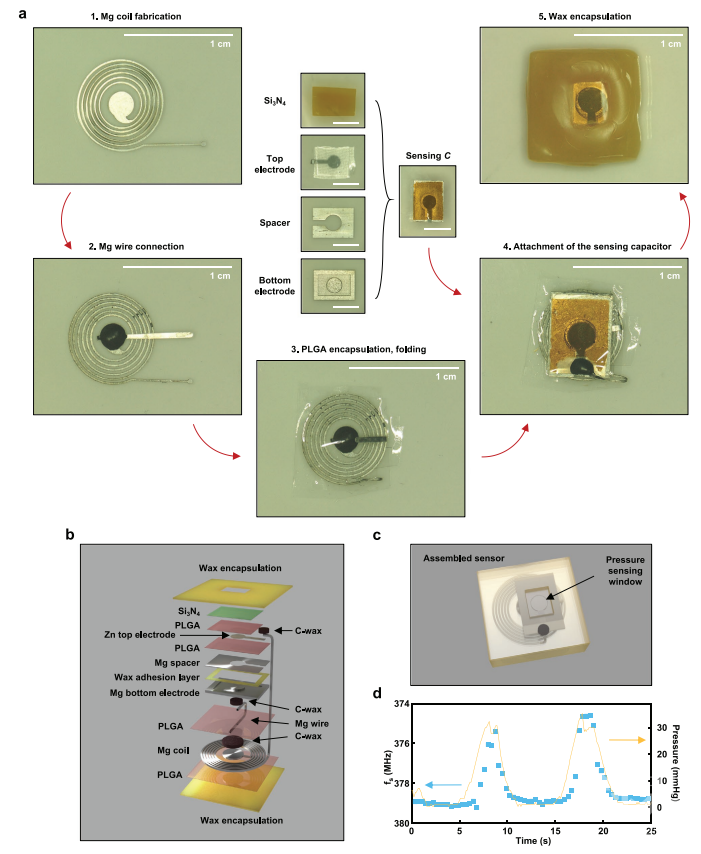 图3:可生物吸收被动式无线压力传感器的制造工艺、结构设计和性能。a) 在制造传感器的各个步骤中收集的光学显微照片。b) 分解图装置示意图。c) 组装的示意图,传感器突出显示电容器上的压力感应窗口。d) 校准曲线:体外测量和压力作为时间的函数。这些装置的结构包括线圈感应器和电容传感器,并用绝缘层作为隔水屏障。首先,采用激光切割镁箔,制作螺旋线圈感应器(100µm厚;图3a)和电容器组件(底部电极250µm;间隔100µm),将激光切割的锌箔(2µm)夹在两层聚乳酸-羟基乙酸共聚物(PLGA)(每层5µm)之间,然后热压,加工出顶部的柔性电极(图3a,中心)。然后进行电容式传感器的组装:用堪地里拉蜡(一种生物相容性蜡)连接底部电极和间隔棒,并通过用乙酸乙酯蒸汽处理PLGA底层的底表面来粘附上电极,以提高与间隔棒的粘合性。最后使用导电蜡(钨粉和堪地里拉蜡的混合物)将线圈与传感器电连接,产生LC谐振电路(图3a)。在上电极上层压一层Si3N4(2µm)的独立膜,并在传感器周围涂覆一层生物相容性蜡(≈500µm),完成制造。工作性能:Si3N4和蜡制作的生物可吸收的生物体液隔膜可在体内稳定运行4天。系统试验表明,所得传感器的性能可达到商用植入式传感器的响应水平,与用于监测颅内压力升高值(ICP)的临床标准设备相当。
图3:可生物吸收被动式无线压力传感器的制造工艺、结构设计和性能。a) 在制造传感器的各个步骤中收集的光学显微照片。b) 分解图装置示意图。c) 组装的示意图,传感器突出显示电容器上的压力感应窗口。d) 校准曲线:体外测量和压力作为时间的函数。这些装置的结构包括线圈感应器和电容传感器,并用绝缘层作为隔水屏障。首先,采用激光切割镁箔,制作螺旋线圈感应器(100µm厚;图3a)和电容器组件(底部电极250µm;间隔100µm),将激光切割的锌箔(2µm)夹在两层聚乳酸-羟基乙酸共聚物(PLGA)(每层5µm)之间,然后热压,加工出顶部的柔性电极(图3a,中心)。然后进行电容式传感器的组装:用堪地里拉蜡(一种生物相容性蜡)连接底部电极和间隔棒,并通过用乙酸乙酯蒸汽处理PLGA底层的底表面来粘附上电极,以提高与间隔棒的粘合性。最后使用导电蜡(钨粉和堪地里拉蜡的混合物)将线圈与传感器电连接,产生LC谐振电路(图3a)。在上电极上层压一层Si3N4(2µm)的独立膜,并在传感器周围涂覆一层生物相容性蜡(≈500µm),完成制造。工作性能:Si3N4和蜡制作的生物可吸收的生物体液隔膜可在体内稳定运行4天。系统试验表明,所得传感器的性能可达到商用植入式传感器的响应水平,与用于监测颅内压力升高值(ICP)的临床标准设备相当。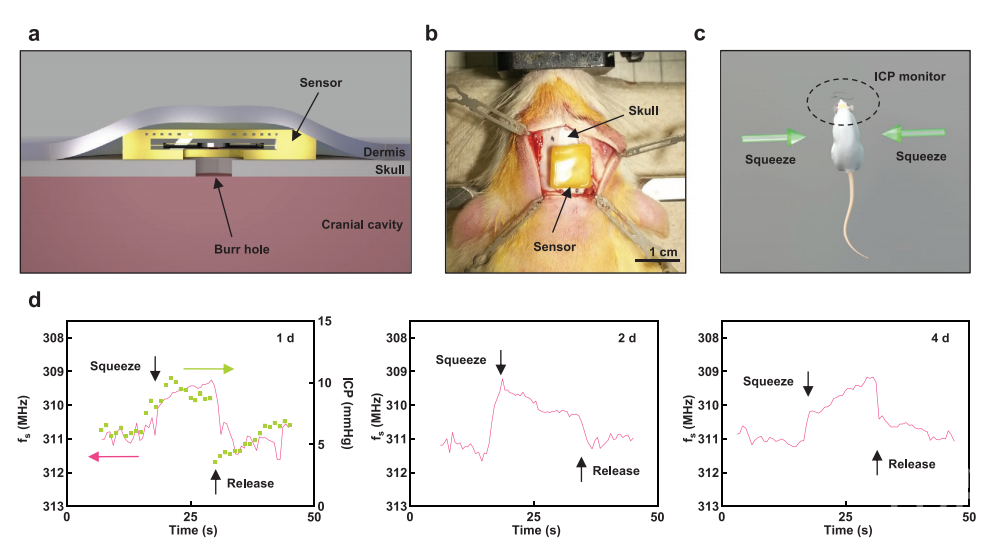 图4: 在大鼠模型上无线测量颅内压。a) 传感器横截面示意图,显示其位于穿过颅骨的毛刺孔上,以便与颅内空间内的液体耦合。b) 缝合手术部位前植入传感器的图像。c) 挤压动物两侧的过程示意图。d) 植入后1d、2d和4d使用生物可吸收无线传感器测量ICP,1d使用商用有线传感器进行相应测量。为了将机械损伤和感染等健康风险降至最低,在1d后取出有线商用ICP传感器。该装置的一个关键特征是所有组成材料都是可生物溶解的。图4显示了37℃下磷酸盐缓冲盐水中的相关化学和物理过程:镁和锌与水反应形成可溶氢氧化物,导电蜡中的钨在水中氧化生成可溶性酸,氮化硅与水反应生成硅酸和氨,PLGA水解为乳酸和乙醇酸并溶解,而生物相容性蜡在体内降解缓慢。
图4: 在大鼠模型上无线测量颅内压。a) 传感器横截面示意图,显示其位于穿过颅骨的毛刺孔上,以便与颅内空间内的液体耦合。b) 缝合手术部位前植入传感器的图像。c) 挤压动物两侧的过程示意图。d) 植入后1d、2d和4d使用生物可吸收无线传感器测量ICP,1d使用商用有线传感器进行相应测量。为了将机械损伤和感染等健康风险降至最低,在1d后取出有线商用ICP传感器。该装置的一个关键特征是所有组成材料都是可生物溶解的。图4显示了37℃下磷酸盐缓冲盐水中的相关化学和物理过程:镁和锌与水反应形成可溶氢氧化物,导电蜡中的钨在水中氧化生成可溶性酸,氮化硅与水反应生成硅酸和氨,PLGA水解为乳酸和乙醇酸并溶解,而生物相容性蜡在体内降解缓慢。 图4压力传感器在37°C 生理盐水中的降解(溶液每2天更新一次)。亮点小结:Rogers团队研制的传感器完全由生物可吸收材料构成,在一定时间段内可稳定运行,但最终完全溶解在生物体液中,从而避免了商业同类产品所需的提取手术。用于传感的无源LC谐振机制实现无电池操作,传感器结构简单。改进压力相关电容器的设计,即增加空气腔的体积和减少寄生电容,可以达到临床应用所需的精确度和精密度。投稿模板:单篇报道:上海交通大学周涵、范同祥《PNAS》:薄膜一贴,从此降温不用电!系统报道:加拿大最年轻的两院院士陈忠伟团队能源领域成果集锦历史进展:经典回顾| 聚集诱导发光的开山之作:一篇《CC》,开启中国人引领世界新领域!
图4压力传感器在37°C 生理盐水中的降解(溶液每2天更新一次)。亮点小结:Rogers团队研制的传感器完全由生物可吸收材料构成,在一定时间段内可稳定运行,但最终完全溶解在生物体液中,从而避免了商业同类产品所需的提取手术。用于传感的无源LC谐振机制实现无电池操作,传感器结构简单。改进压力相关电容器的设计,即增加空气腔的体积和减少寄生电容,可以达到临床应用所需的精确度和精密度。投稿模板:单篇报道:上海交通大学周涵、范同祥《PNAS》:薄膜一贴,从此降温不用电!系统报道:加拿大最年轻的两院院士陈忠伟团队能源领域成果集锦历史进展:经典回顾| 聚集诱导发光的开山之作:一篇《CC》,开启中国人引领世界新领域!


 微信公众号
微信公众号
 下载app
下载app
 京公网安备 11010202008974号
京公网安备 11010202008974号