来源:CBG资讯
生物大分子可以控制活细胞中的一系列生物转化过程,比人工生物系统具有更高的效率、特异性和选择性。由于生物大分子固有的脆弱性,采用生物大分子(例如酶)进行无细胞生物转化过程通常需要将其固定在多孔载体中。金属有机骨架(MOFs)是一类由金属节点和有机配体组装而成的多孔材料,具有超高的表面积、可定制的孔隙率和特定的骨架组成。MOFs的超高孔隙率为宿主生物分子提供了类似细胞膜的结构,而开放的MOFs网络则允许在活细胞中选择性转运模拟生物转化过程的底物。
3D沸石咪唑酯骨架(ZIF,~3.5 Å孔径)是研究最广泛的用于容纳生物实体的MOFs,这是由于它们具有生物相容性较好的合成条件,可防止生物大分子在MOFs生物复合体形成过程中变性。为了提高MOFs生物复合体的生物功能性,迫切需要了解MOFs结构对宿主生物大分子活性的作用,以促进构建高活性的MOF生物复合体。
近期,中山大学欧阳钢锋教授课题组报道了一种实用且生物相容的策略来增强生物分子的生物活性。该策略将ZIF-8包裹的生物复合体制备为可控的纳米结构,形成的ZIF-8涂层可以通过肽调节剂γ-聚-L-谷氨酸(PLGA)从不同的3D微孔结构转换为2D中孔层。PLGA是一种富含羧基的生物相容性阴离子多肽,通常用作生物大分子的表面改性剂,可显著促进生物大分子周围MOFs的形成。同时,多余的PLGA链可以通过羧基与金属离子的竞争性配位作用,导致复合材料的形貌演变并生成缺陷结构(图一)。基于这种策略,作者全面评估MOFs纳米结构对生物大分子活性的影响,证明了生物大分子封装在新型2D介孔纺锤形的MOFs架构(2D MSMOFs)中可以大大提高MOFs生物复合体的活性。这是由于在2D MSMOFs中扩散路径的缩短和孔道的扩大促进了生物转化过程中的相互交换。此外,2D MSMOFs薄层还通过结构限制对宿主生物大分子及其蛋白质支架的生物矿物质提供出色的保护作用,从而使它们能够在生活环境中发挥其生物学功能。相关成果以“Embedding Functional Biomacromolecules within Peptides-Directed Metal-Organic Frameworks Nanoarchitectures Enables Activity Enhancement”为题发表在国际化学权威杂志Angew. Chem. Int. Ed.上(DOI: 10.1002/anie.202005529)。
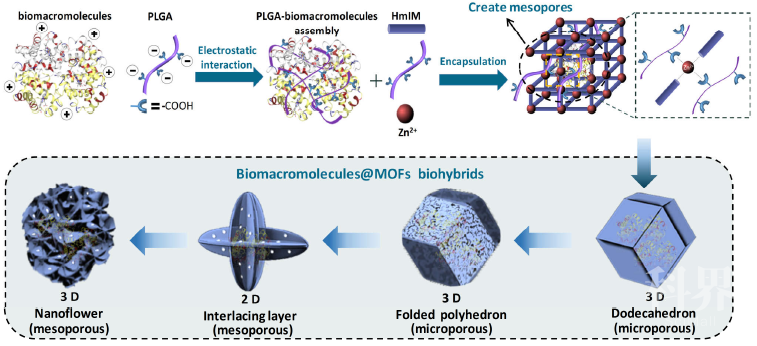
图一、通过PLGA调节将生物大分子原位封装在可变形MOFs中的示意图
(来源:Angew. Chem. Int. Ed.)
首先,作者以辣根过氧化物酶(HRP)作为生物大分子模型,研究了多肽介导的MOFs生物复合体的形态演化过程。HRP是一种铁血红素酶,可催化底物被过氧化氢氧化。在典型的封装过程中,将HRP分散到多肽水溶液中,然后添加金属离子(醋酸锌)和2-甲基咪唑(HmIM)。将混合物陈化,然后形成生物大分子 @MOFs生物复合物。生物大分子氨基酸残基中羧基所带的负电荷在加速生物大分子周围MOFs的形成中起着关键作用,但具有正表面电荷的HRP无法诱导MOFs的形成。当引入PLGA时,具有丰富羧基的PLGA通过静电相互作用改性HRP,从而促进了生物大分子@MOFs复合物的形成。这种快速的自我诱导的MOFs形成能够降低封装过程中生物大分子失活的风险。
作者分别用扫描电子显微镜和透射电子显微镜研究了所得复合材料的形貌演变(图二)。当没有PLGA介入的情况下进行封装时,复合材料会长成均匀的3D菱面体十二面体,直径大约为1.5 μm。通过添加1 mg至5 mg PLGA,生物复合物逐渐演变为具有折叠表面的不规则3D多面体(polyhedron)。PLGA剂量的增加导致形态演变为3D十字交叉形(decussation),并最终形成2D纺锤形的层,其厚度大约为150 nm。进一步增加PLGA剂量可将2D层组装成3D花状结构(nanoflower),布拉格衍射峰的相应演变也支持PLGA能够调节生物大分子@MOFs生物复合体的晶体生长,其中典型的3D ZIF-8衍射峰变弱,并伴随着2D层的新衍射峰的出现。作者通过傅里叶变换红外光谱测试验证了掺入的PLGA与金属离子配位,通过X射线光电子能谱测试成功记录了Zn、C、N和O的元素, 其中Zn 2p3高分辨光谱表明了PLGA与Zn2+的竞争配位形成了新的Zn-O键。调节剂的竞争性配位通常能够在MOFs中产生缺陷,氮吸附等温线验证了在生物复合体演变过程中,1.1 nm的微孔转化为2 nm至20 nm的中孔。这些结果证实了PGLA肽调节剂能够调节MOFs生物复合体的纳米结构和孔径大小。

图二、生物大分子@MOFs生物复合物的形貌、晶型表征图
(来源:Angew. Chem. Int. Ed.)
接着,作者研究了MOFs的纳米结构对活性的影响。作者使用3,3',5,5'-四甲基联苯胺(TMB)作为过氧化物酶底物,评估了封装HRP的MOFs纳米结构对所形成的生物复合体活性的影响。其中,HRP@3D微孔MOFs表现出极低的活性,这归因于3D微孔结构中基质的扩散受阻;HRP@2D MSMOF能够瞬间将TMB催化为蓝色产物(oxTMB)。通过全面评估MOFs纳米结构对包封的生物大分子活性的影响,相对酶活性计算如下:HRP@2D MSMOFs > HRP@3Ddecussation MOFs ≈ HRP@3D nanoflower MOFs > HRP@3D polyhedron MOFs。结果表明,二维结构和介孔孔径有利于高活性的保存。为了验证该结论,作者使用细胞色素C(Cyt C)和葡萄糖氧化酶(GOx)在内的其他蛋白质嵌入2D MSMOFs中,以研究其催化活性(图三)。

图三、酶@MOFs复合物活性研究示意图
(来源:Angew. Chem. Int. Ed.)
最后,作者研究了生物催化和刺激响应型MOFs作为细胞模拟物(图四)。受2D MSMOF保护的生物大分子的生物活性以及耐久性的提高增加了其在有机相生物催化中的应用潜力。与HRP@3D MOFs相比,构建的HRP@2D MSMOFs生物催化剂显示出对DMF中芳香族胺催化氧化能力的增强。在细胞环境中的生物催化级联反应代表了主要的化学转化类别,可以使生物信号转导和代谢途径有序地进行。模仿细胞的生物级联反应可以进行局部和程序化的反应过程,该过程已用于新型生物医学应用中,例如微反应器和生物传感器。受到此启发,作者通过将生物识别单元GOx和生物信号传输单元共同限制在2D MSMOFs中,构建了葡萄糖刺激的多反应“细胞模拟物”(CM)。当将葡萄糖添加到构建的2D MSMOFs CM中时,生物级联被激活。葡萄糖首先被GOx识别并催化反应生成H2O2,生成的H2O2充当金纳米团簇(AuCNs)的底物,不仅可以通过牛血清蛋白-金纳米团簇(BSA-AuCNs)的过氧化物酶样活性将TMB催化为oxTMB,而且还可以氧化导致进行荧光猝灭。构建的MSMOFs CM启用了葡萄糖反应性双信号转导:色度“turn-on”和荧光“turn-off”。这两个信号读数的视觉辨别力是互补的,其中色度“turn-on”的敏感区域是1.0-10.0 mM,而荧光“turn-off”的敏感区域是0.1-1.0 mM。另外,作者观察到信号强度和葡萄糖浓度之间的良好线性。这表明通过使用双响应MSMOFs CM可以实现更高分辨率的视觉检测。为了验证2D MSMOFs纳米结构在模仿生物级联通讯方面的优势,作者还使用类似的策略构建了3D微孔MOFs CM。通过葡萄糖激活后的荧光响应率评估的3D微孔MOFs CM中的生物级联通讯比2DMSMOF CM中的生物级联通迅要慢得多,这种对信号响应的抑制归因于在3D微孔结构中生物级联的相互通讯受阻。

图四、MOFs复合物作为细胞模拟物的研究示意图
(来源:Angew. Chem. Int. Ed.)
小结:中山大学欧阳钢锋教授课题组报道了一种生物相容性、肽导向的策略,以简单的方式将覆盖MOFs的生物复合物制备成可控的纳米结构,并强调设计的MOFs构架对于维持所获得的纳米生物复合物生物功能的重要性。与广泛研究的3D微孔MOFs生物复合材料相比,新型2DMSMOFs生物复合物显示出显著的活性增强,这归因于扩散路径的缩短和孔道的扩大。同时,设计的2D MSMOFs涂层赋予嵌入的生物大分子及其生物矿物质以增强的生物功能性,并允许其在不宜居住的条件下进行模拟细胞的活动。该发现为构建具有出色生物活性和耐久性的功能性MOFs生物系统提供了新的见解,这可能会推动人工细胞的构建并加速复杂应用中无细胞的生物转化。







 下载app
下载app